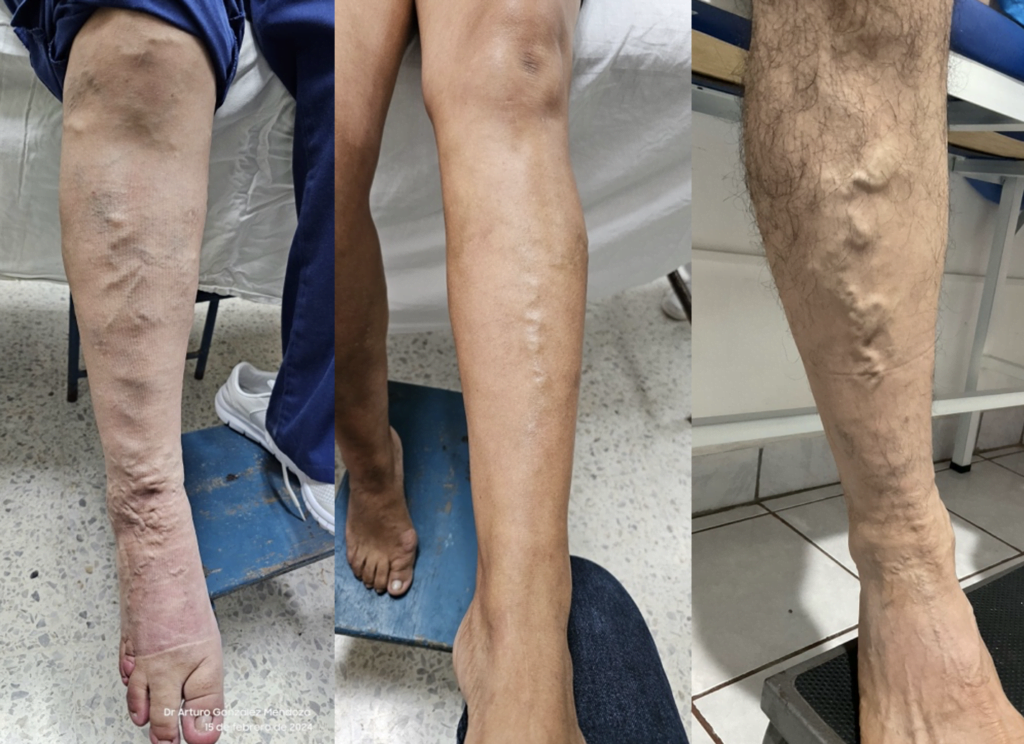
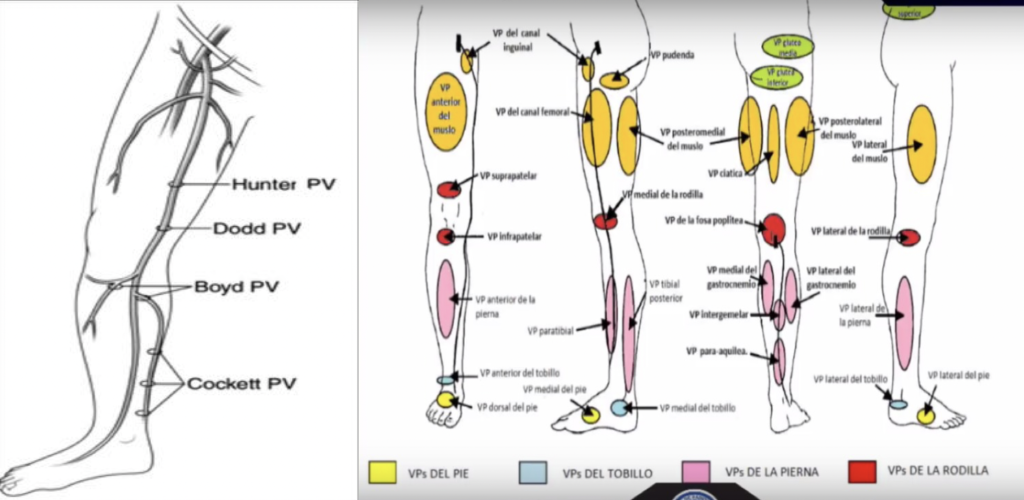
EFECTO DE LAS PLASMA RICO EN PLAQUETAS SOBRE UNA ÚLCERA CUTÁNEA EN PACIENTE CON SÍNDROME DE SHEEHAN
Palabras clave:
Úlcera cutánea, plasma rico en plaquetas, esteroides, Síndrome de Sheehan.
Key words:
Skin ulcer, platelet-rich plasma, RHYNS syndrome,
RESUMEN
Las heridas crónicas siempre representan un reto, más aún cuando hay factores agravantes como la toma de esteroides crónicamente por una enfermedad de base. Éstos pueden atrofiar la piel y disminuir la cicatrización. La paciente del caso presenta un síndrome de Sheehan, mas hipotiroidismo de más de 30 años de evolución, tiempo desde el cual ha estado tomando esteroides para controlar las patologías. La paciente sufre un traumatismo en la pierna, provocando una úlcera que no cerraba con los métodos convencionales. Se utilizó plasma rico en plaquetas en forma de gel para ayudar al cierre más rápido de la úlcera. El objetivo es mostrar al plasma rico en plaquetas como una alternativa barata y de fácil acceso para la cicatrización de heridas difíciles.
INTRODUCCIÓN
Las úlceras en las extremidades inferiores crónicas son heridas localizadas en las piernas o en los pies1 que no completan su proceso de reparación hasta lograr la integridad anatómica y funcional del tejido2, , sin embargo, no existe un consenso sobre el tiempo en el que este debe completar3, ya que algunos autores expresan un período de dos a cuatro semanas3–5, mientras que otros, se refieren a seis semanas y hasta tres meses esta falta de definición de criterios dificulta el diagnóstico y el cálculo de la prevalencia6,.
La incidencia y prevalencia de las heridas crónicas se ha incrementado debido al aumento de las enfermedades crónicas y al envejecimiento de la población3,7, a lo que también contribuyen las hospitalizaciones y la institucionalización8. Este es un problema de salud que representa una carga económica y asistencial para los sistemas de salud, afecta la calidad de vida principalmente, de los adultos mayores9 y aumenta el riesgo de muerte10,
Se estima que las ulceras de miembros inferiores afectan a más de 49 millones de personas a nivel mundial con una incidencia de tres a cinco casos nuevos por mil personas10, con una prevalencia entre 0,1 a 0,30 %, que puede llegar hasta el 4 %. Se estima que las ulceras en los miembros inferiores se presentan en 1 a 2 % de la población adulta de Estados Unidos11.
Las principales causas de las ulceras crónicas son los problemas vasculares (entre el 50 y el 70%) y otras como la diabetes mellitus, la hipertensión arterial los traumatismos, la obesidad y los traumatismos12.
Los tratamientos más recomendados se basan en las guías de práctica clínica de Servicio Valenciano de Salud, de Canadá, Reino Unido, Australia y Bélgica13.
Uso de plasma rico en plaquetas14–16
El plasma rico en plaquetas (PRP) es un hemoderivado con un alto recuento de plaquetas, que puede ser producido por varias centrifugaciones, y aunque no hay un protocolo universal sobre cómo preparar el PRP se indica que debe tener al menos 2.5-1000 x103 plaquetas/μL(de 2 a 7 veces el valor basal), aunque un reciente meta análisis describe como optima la concentración de plaquetas 1.0 x106 /μL.
Los factores de crecimiento plaquetario se encuentran concentrados en el plasma rico en plaquetas (PRP), el cual es de fácil preparación y sin necesidad de equipo costoso. El PRP dentro de sus efectos tiene activar los fibroblastos, aumentar la producción de colágeno, elastina y ácido hialurónico, consiguiendo una mejora en general de la calidad de la piel. Además, promueve el crecimiento, coagulación, proliferación y diferenciación celular, constituyendo por tanto el inicio de la reparación tisular, ayudando además en las tres fases de la cicatrización, inflamación, proliferación, y remodelación; así como para matar patógenos, remover tejido necrótico y favorecer la cicatrización.
Los tratamientos para las heridas crónicas, es muy variado y se basa principalmente en la utilización de apósitos, y en el tratamiento de la causa para lograr la cicatrización. Pero existen casos en los que no es posible eliminar la causa, como en un trauma, y en los que no es posible eliminar los factores de cronicidad de la úlcera como el uso crónico de esteroides, sin correr riesgo de agravar una condición previamente existente.
Los factores de crecimiento son una familia de señales peptídicas moleculares capaces de modificar las respuestas biológicas celulares. Son mediadores biológicos que regulan la migración, la proliferación, diferenciación y metabolismo celular. Los factores de crecimiento asociados al PRP son: PDGF (factor de crecimiento asociado a plaquetas), TGF-B (Factor de crecimiento transformante beta), VEGF (factor de crecimiento endotelial vascular), IGF-1 (factor de crecimiento similar a insulina), HGF (factor de crecimiento de hepatocito). La concentración de factores de crecimiento es directamente proporcional a la cantidad de plaquetas, por lo tanto, el PRP, que es un concentrado de plaquetas de al menos 6 veces su cantidad normal, proporcionará grandes cantidades de estos factores favoreciendo la cicatrización de heridas tórpidas.
El plasma fue obtenido mediante sangre venosa, fue colocado en un tubo de ensayo sin anticoagulante, en donde previamente se había colocado 1 gm de vitamina C líquida. Todo esto se centrifugó a 1,800 rpm durante 8 minutos, con doble centrifugación. Al obtener el plasma, se separa el PRP del resto, se activa mediante burbujeo de ozono a 80 mg/Nml en relación 1:1, luego se coloca en otro tubo de ensayo sin anticoagulante y se expone al calor mediante baño de maría, con agua a la temperatura del oasis (servidor de agua potable), durante 5 minutos, o hasta corroborar que se había gelificado. Al estar en forma de gel, se extrae y se coloca con una jeringa sobre el lecho de la herida, se cubre con apósito de espuma y se fija mediante adhesivo. El plasma fue colocado cada 7 días en tres ocasiones consecutivas.
Los pacientes con SHH no están exentos de sufrir traumas y heridas, pero ante el uso crónico de esteroides se necesita una aproximación diferente que tome en cuenta los efectos secundarios de los mismos. En este caso mostramos cual fue el efecto de plasma rico en plaquetas (PRP) como una estrategia para disminuir el efecto secundario del esteroide y lograr la cicatrización en el menor tiempo posible, en un paciente con úlcera traumática con Síndrome de Sheeham.
Este caso nos muestra el efecto del uso de plasma rico en plaquetas en una herida crónica en un paciente tratado crónicamente con esteroides.
PRESENTACIÓN DEL CASO
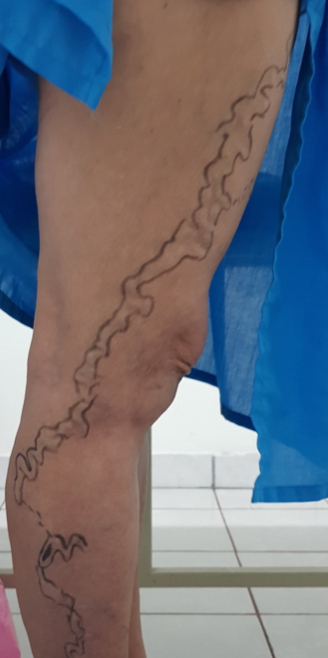
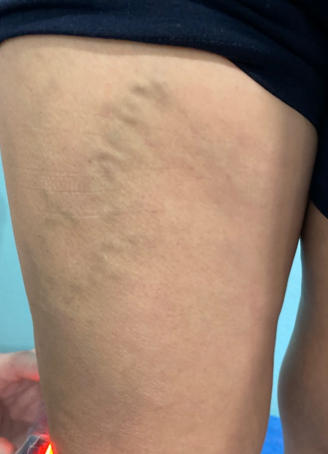
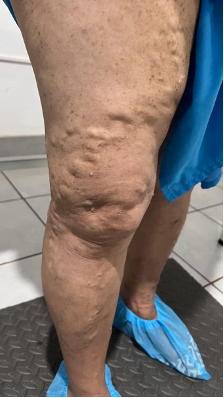
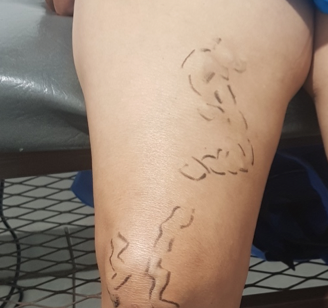
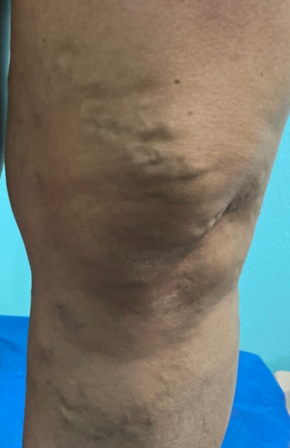
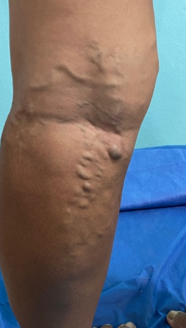
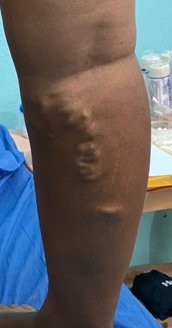
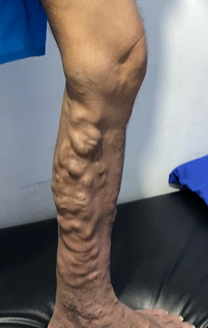
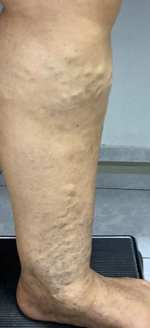
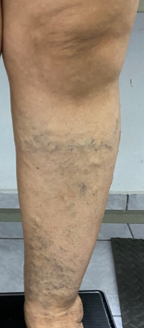
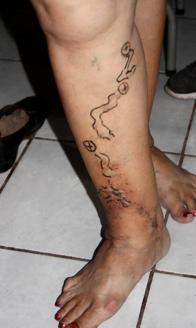
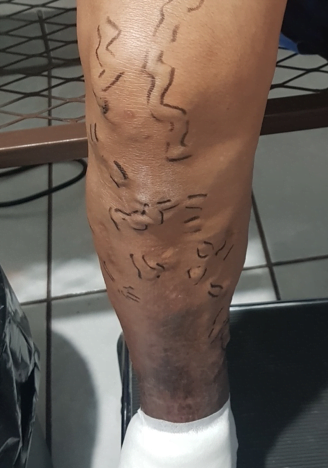
Se trata de una paciente femenina de 83 años, con historia de cuatro semanas de haber sufrido un traumatismo en pierna derecha, con la rama de un árbol, fue automedicada con penicilina tópica y otros remedios caseros que no recuerda, cuando no observó mejoría decidió consultar. Expresó tener antecedentes de síndrome de Sheehan, desde hace 30 años, e hipotiroidismo secundario tratada con prednisona 10 mg al día y levotiroxina 100 mg al día. Además, una resección de cáncer basocelular en la mejilla derecha, hace diez años con nueva lesión hace 5 años, ya tratada con extirpación completa por cirujano plástico.
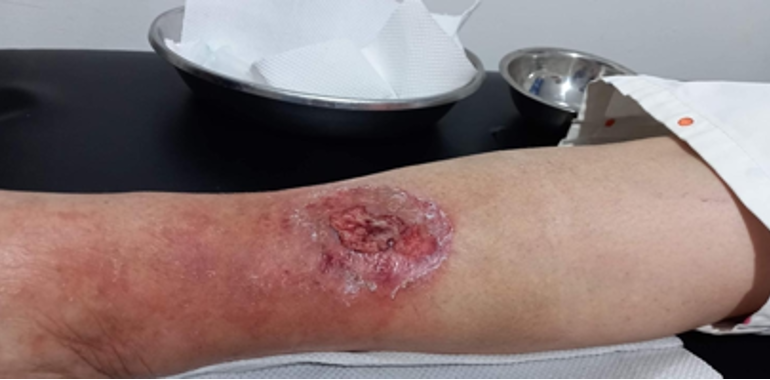
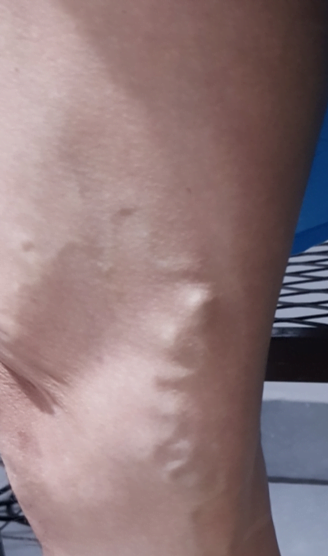
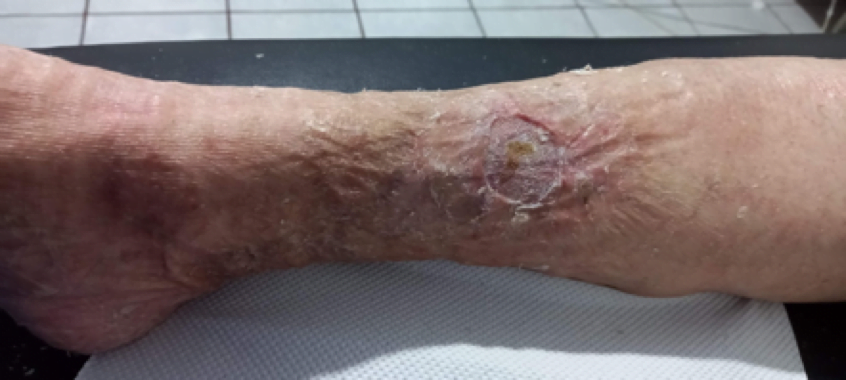
Se realizó la evaluación física, la paciente caminaba con dificultad, presentaba edema del miembro inferior derecho, con índice tobillo-brazo de 0,90. Se evaluó el área de la lesión, donde presentó una úlcera de 4 cm × 2,5 cm (Figura 1). Se realizó evaluación del lecho de la herida se aplica la estrategia TIME se observa signos de colonización local.
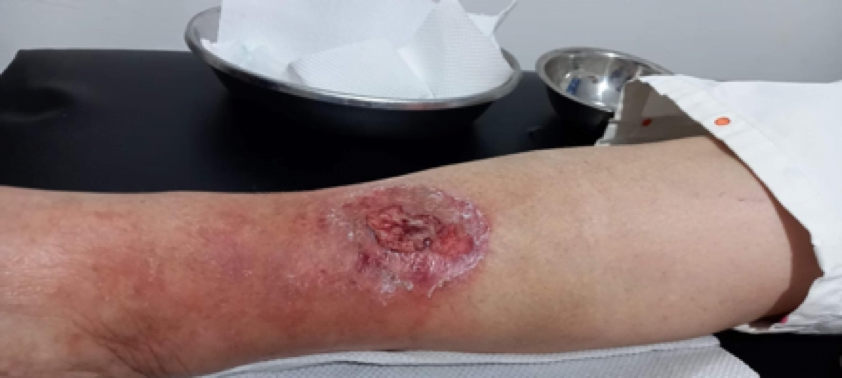
Se le indicaron exámenes de laboratorio en los que se encontraba con leucocitosis, con dislipidemia leve, hemoglobina, hematócrito, glucosa, albúmina y fibrinógeno dentro de los valores normales y proteína C cuantitativa negativa (Tabla 1).
Tabla 1. Exámenes de laboratorio
| Examen | Resultado |
| Hemoglobina | 12,9 |
| Hematocrito | 36,9 % |
| Glóbulos blancos | 24 290 mm3 |
| Creatinina | 0,96 mg/dl |
| Hemoglobina glicosilada | 5,9 % |
| Albúmina sérica | 3,9 gr/dl |
| Colesterol total | 202 mg/dl |
| Triglicéridos | 297 mg/dl |
| Colesterol de baja densidad | 93,4 mg/dl |
| Colesterol de alta densidad | 49,2 mg/dl |
| Fibrinógeno | 125,0 mg/dl |
| Proteína C cuantitativa | negativo |
Intervención terapéutica
Se realizó una curación cada semana, durante 8 semanas semanas, la curación consistía en el desbridamiento cortante de la herida, seguido de la colocación de una gasa con agua ozonizada a 80 ųg/NmL, luego se colocaba la extremidad dentro de una bolsa plástica durante 15 minutos para la colocación de ozono tópico, posteriormente se colocaba el apósito hidropolimérico de plata. En la 4 semana, se sustituyó la colocación del apósito por la aplicación de PRP y la colocación posterior de un apósito secundario.
Se aplicó compresión terapéutica multicomponente con almohadillado y 1 venda de baja elasticidad aproximada de unos 32 mmHg aplicada desde la base de los dedos hasta debajo de la rodilla para conseguir un gradiente de presión lo suficientemente efectivo como para controlar el edema y se le indicó a la paciente que deambulara.
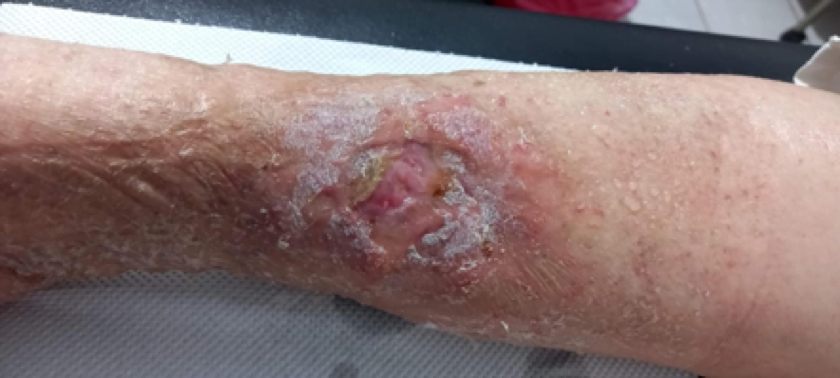
DISCUSIÓN
El uso crónico de esteroides tiene muchos efectos secundarios ampliamente conocidos; las alteraciones en la cicatrización provocadas por éstos es algo que no se ha tomado en cuenta en los pacientes con uso de por vida de este medicamento como con el síndrome de Sheeham, El tratamiento etiológico de la úlcera es fundamental para lograr su cicatrización, Existen varios factores que impiden o retrasan la cicatrización entre ellos se pueden mencionar el uso de esteroides.
Los efectos secundarios de los esteroides son bien conocidos pero hay uno que interesa en el caso de la cicatrización el cual es la inhibición de la inflamación y supresión de la respuesta inmunitaria; ambos podrían llevar a la cronicidad de una herida independientemente de la causa de ésta, Estudios sobre cómo afecta la prednisona a la cicatrización en pacientes con trasplantes de pulmón encontró índice de colágeno significativamente menor que en los grupos de comparación (4), Aunque existen estudios que indican que la prednisona a dosis de 0,5 mg/kg/día no tienen efecto sobre la cicatrización en heridas abdominales experimentales. Los efectos de los esteroides en la piel y los tejidos blandos pueden ser atrofia dérmica aparición de púrpura acné hipertricosis alopecia estrías aumento de la frecuencia de cáncer de piel (pero no de melanoma) así como la reparación de heridas asépticas es inhibida por los corticoides.
Los efectos secundarios de los esteroides son bien conocidos pero hay uno que interesa en el caso de la cicatrización el cual es la inhibición de la inflamación y supresión de la respuesta inmunitaria; ambos podrían llevar a la cronicidad de una herida independientemente de la causa de ésta, Estudios sobre cómo afecta la prednisona a la cicatrización en pacientes con trasplantes de pulmón encontró índice de colágeno significativamente menor que en los grupos de comparación. Aunque existen estudios que indican que la prednisona a dosis de 0,5 mg/kg/día no tienen efecto sobre la cicatrización en heridas abdominales experimentales. Los efectos de los esteroides en la piel y los tejidos blandos pueden ser atrofia dérmica aparición de púrpura acné hipertricosis alopecia estrías aumento de la frecuencia de cáncer de piel (pero no de melanoma) así como la reparación de heridas asépticas es inhibida por los corticoides.
La paciente obtuvo epitelización del 100% del lecho de la herida en tres semanas luego de iniciada la colocación de PRP siendo seguro sin riesgo de infección o transmisión de enfermedades. En numerosos estudios se ha reconocido que el PRP mejora y acelera la regeneración de los tejidos donde se aplica, sin efectos secundarios conocidos, Es capaz de Aún con los efectos adversos del uso crónico de esteroides, La colocación del PRP en úlceras es una terapia complementaria barata de fácil aplicación que acelera de forma segura la epitelización de los pacientes por lo que debería estar disponible en todas las clínicas que se dediquen a la curación de úlceras,
ASPECTOS ÉTICOS
Se ha respetado la confidencialidad de la paciente así como el uso de sus datos personales, Se obtuvo el consentimiento informado para la escritura de este caso,
Referencias bibliográficas
1, Singer AJ Tassiopoulos A Kirsner RS, Evaluation and Management of Lower-Extremity Ulcers Campion EW editor, N, Engl, J, Med, 2017;377(16)1559–1567, doi10,1056/NEJMra1615243
2, Lazarus GS Cooper DM Knighton DR Margolis DJ Percoraro RE Rodeheaver G Robson MC, Definitions and guidelines for assessment of wounds and evaluation of healing, Wound Repair Regen, 1994;2(3)165–170, doi10,1046/j,1524-475X,1994,20305,x
3, Kyaw B Järbrink K Martinengo L Car J Harding K Schmidtchen A, Need for Improved Definition of ”Chronic Wounds” in Clinical Studies, Acta Derm, Venereol, 2018;98(1)157–158, doi10,2340/00015555-2786
4, Leaper DJ Durani P, Topical antimicrobial therapy of chronic wounds healing by secondary intention using iodine products, Int, Wound J, 2008;5(2)361–368, doi10,1111/j,1742-481X,2007,00406,x
5, Sen CK, Human Wounds and Its Burden An Updated Compendium of Estimates, Adv, Wound Care, 2019;8(2)39–48, doi10,1089/wound,2019,0946
6, Dubhashi SP Sindwani RD, A Comparative Study of Honey and Phenytoin Dressings for Chronic Wounds, Indian J, Surg, 2015;77(S3)1209–1213, doi10,1007/s12262-015-1251-6
7, Wicke C Bachinger A Coerper S Beckert S Witte MB Königsrainer A, Aging influences wound healing in patients with chronic lower extremity wounds treated in a specialized wound care center, Wound Repair Regen, 2009;17(1)25–33, doi10,1111/j,1524-475X,2008,00438,x
8, da Rosa Silva CF Santana RF de Oliveira BGRB do Carmo TG, High prevalence of skin and wound care of hospitalized elderly in Brazil a prospective observational study, BMC Res, Notes, 2017;10(1)81, doi10,1186/s13104-017-2410-6
9, Posnett J Franks PJ, The burden of chronic wounds in the UK, Nurs, Times, 2008;104(3)44–45,
10, Salenius J Suntila M Ahti T Huhtala H Vaalasti A Salmi T Kimpimäki T, Long-term Mortality among Patients with Chronic Ulcers, Acta Derm, Venereol, 2021;101(5)adv00455, doi10,2340/00015555-3803
11, Alavi A Sibbald RG Phillips TJ Miller OF Margolis DJ Marston W Woo K Romanelli M Kirsner RS, What’s new Management of venous leg ulcers, J, Am, Acad, Dermatol, 2016;74(4)627–640, doi10,1016/j,jaad,2014,10,048
12, Werdin F Tennenhaus M Schaller H-E Rennekampff H-O, Evidence-based management strategies for treatment of chronic wounds, Eplasty, 2009;9e19,
13, Quality of clinical practice guidelines on deterioration of skin integrity, An, Sist, Sanit, Navar, 2017;40(3)489–490, doi10,23938/ASSN,0116
14, De la Torre Barbero MJ Estepa Luna MJ Rubio Moreno J, Uso del Plasma Rico en Plaquetas para el tratamiento de las úlceras de miembro inferior, Estudio piloto, Revista de Enfermería Vascular, 2020;3(6)15–21,
15, Castro-Piedra SE Arias-Varela KA, Actualización en plasma rico en plaquetas, Acta Médica Costarricense, 2019;61(4)142–151,
16, Carter MJ Fylling CP Parnell LKS, Use of platelet rich plasma gel on wound healing a systematic review and meta-analysis, Eplasty, 2011;11e38,
17, Díaz Herrera MÁ Baltà Domínguez L Blasco García MC Fernández Garzón M Fuentes Camps EM Gayarre Aguado R Girona Zaguirre M, Manejo y tratamiento de úlceras de extremidades inferiores, 2020,
18, Rahim K Saleha S Zhu X Huo L Basit A Franco OL, Bacterial Contribution in Chronicity of Wounds, Microb, Ecol, 2017;73(3)710–721, doi10,1007/s00248-016-0867-9